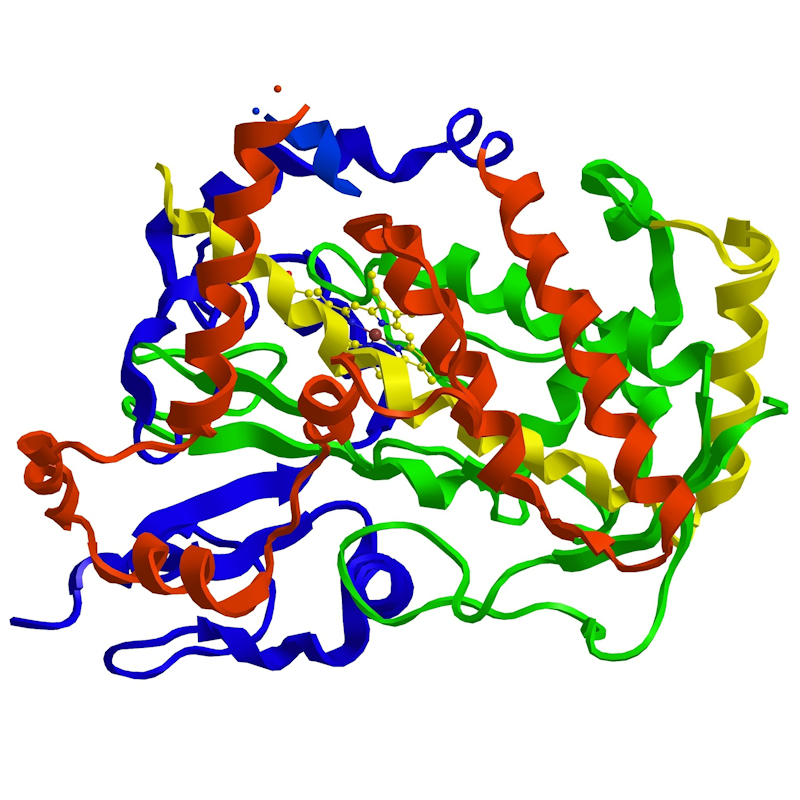
合理的ドラッグデザインのための巨大分子の3D構造解析
この技術は、単結晶構造解析X線回折(SXRD)を用いて大きな生物学的分子の三次元構造を明確に決定するものです。 製薬およびバイオテクノロジーの研究では、タンパク質および関連巨大分子内において分子レベルで疾患がどのように制御されているかを解明し、その知識に基づいて特定の実体を標的にすることが必要です。 このアプローチをとるためには、調べたい巨大分子の高分解能3D分子構造を得ることが前提になります。 この研究の重要性を考えたとき、リガクは巨大分子結晶学のさまざまな側面に関連する幅広い機器の開発において最先端にいるといえます。
タンパク質構造の位相解析 Cr線源を用いて、位相問題をラボ機で解く
単波長異常分散法(SAD法)は、放射光のデータからタンパク質の構造を解くために頻繁に使用される方法で、放射光の波長可変性を利用して金属の吸収端付近の重原子誘導体を測定するものです。 メチオニン含有タンパク質の場合、セレノメチオニン誘導体を調製して、Seの異常分散が利用されます。
しかしながら、SeMet誘導体として結晶化しないタンパク質もあり、また全てのタンパク質がメチオニンを含有するわけでもありません。 その一方、硫黄は、ほとんどすべてのタンパク質のシステイン残基に存在しています。 SeMet置換や重原子浸漬が不要であれば、タンパク質X線結晶構造解析のプロセスは大幅に簡素化されます。 クランビンの構造は、硫黄の異常分散を用いた単波長異常散乱法(S-SAD法)を用い、CuKα線を使用したデータから1981年に解析されました。また、他の多くのタンパク質の構造も、Cu線またはCu線近傍の波長に調整された放射光を用いて解析されました。
医学、バイオテクノロジーおよび薬理学において、創薬とは、薬物を発見し設計するプロセスです。 最近まで、ほとんどの薬は伝統的な治療法から有効成分を特定することによって、あるいは偶然の発見によって発見されてきました。 これに対し、いわゆる「合理的ドラッグデザイン」を用いた新しいアプローチは、疾患および感染が分子的および生理学的レベルでどのように制御されているかを理解し、この知識に基づいて特定の実体をターゲットにするというものです。 この重要な分野、高分子および低分子構造決定のための単結晶回折の開発において、リガクは最先端であり続けているといえます。 リガクの製品は、結晶の回折によるスクリーニングや高解像度データ収集システムから3D構造精密化およびイメージングソフトウェアまで多岐にわたります。